文 / 徐泰浩 博士
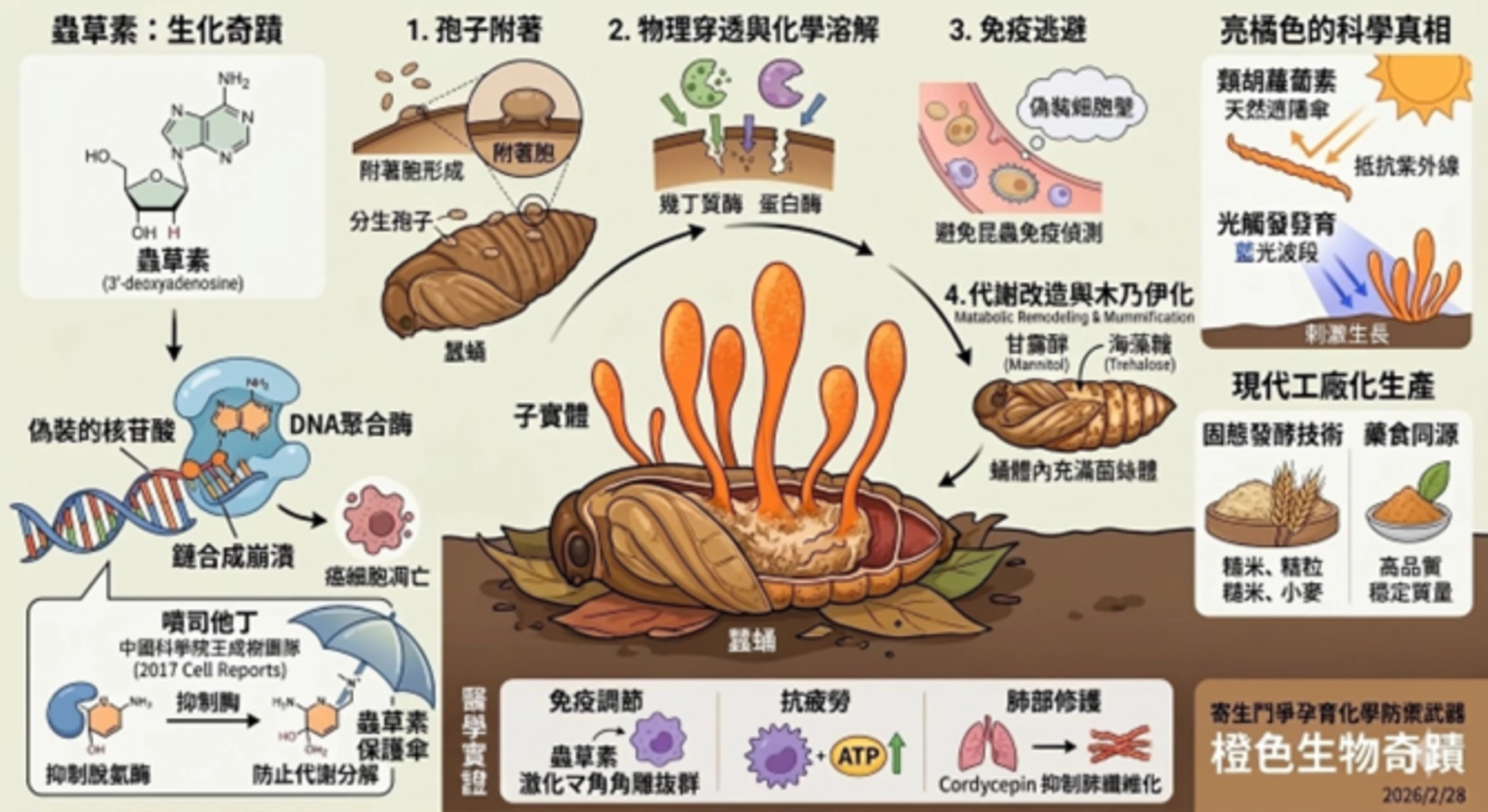
這篇文章將帶你進入一場微觀世界的「奪捨」大戲。我們常在電影或遊戲《最後生還者》(The Last of Us)中看到令人毛骨悚然的「殭屍真菌」,但現實中,蛹蟲草(Cordyceps militaris)的故事遠比虛構更加精彩且充滿正能量。這不只是一場關於寄生的殘酷童話,更是一次生物化學的奇蹟變身。
導讀:從恐怖片主角到生技界的「橙色黃金」
如果你在野外的落葉層下,發現一個金黃色、像是小鹿角般的真菌破土而出,別懷疑,你正目睹一場長達數週的「代謝改造工程」的終點。這就是蛹蟲草。
長期以來,它被視為「冬蟲夏草」的平替版,但在現代科學家眼中,蛹蟲草更像是一個「高效能生物工廠」。它不僅擁有獨特的寄生美學,其產出的活性物質「蟲草素(Cordycepin)」更是目前抗癌與抗病毒研究的明星分子。本篇文章將透過演化生物學、基因組學與藥理學的視角,為你揭開這隻「殭屍真菌」華麗轉身的科學真相。
奪命之吻:精準的「生化入侵術」
蛹蟲草的一生,始於一顆肉眼看不見的孢子。當這顆孢子偶然落在鱗翅目昆蟲(如蠶蛹)的表皮上時,一場無聲的戰爭就此爆發。
- 物理破壁與化學強酸
孢子並非直接「吃」掉昆蟲,它會先特化出附著胞(Appressorium)*1 的構造,產生極高的物理壓力,並配合分泌幾丁質酶(Chitinases)與蛋白酶。這就像是用化學藥劑溶解保險箱門鎖,同時用強大的千斤頂撬開空隙。
*1 當蛹蟲草的分生孢子(Conidia)附著在昆蟲(如家蠶蛹)體表後,會萌發出發芽管。在接觸到適宜的物理信號(如粗糙度)或化學信號時,發芽管頂端會膨大形成球狀或卵圓形的附著胞。附著胞會分泌胞外黏質(ECM),將自身牢牢固定在昆蟲體表,防止被雨水沖刷或寄主活動甩落。
研究證實,蛹蟲草分泌多種幾丁質酶和蛋白酶來分解基質,這些酶的轉錄水平和酶活性在子實體發育過程中顯著增加 [1,2]。幾丁質酶在感染過程和子實體發育中發揮關鍵作用 [3,4]。
- 逃避偵測的「隱身術」
一旦進入昆蟲體內,蛹蟲草會展現出高超的偽裝。研究顯示,它能改變細胞壁的成分,躲過昆蟲免疫系統的偵測。昆蟲的類白血球功能血細胞完全沒意識到,這個外來者正潛伏在它的血液(血淋巴)中吸取養分 [5]。
傀儡大師:代謝系統的「強制接管」
這正是「殭屍真菌」名號的由來。與一般直接殺死宿主的細菌不同,蛹蟲草需要宿主「活得久一點」。
- 營養轉化中心
蛹蟲草感染昆蟲宿主後,會分泌蛋白酶、脂肪酶及幾丁質酶等胞外酶,降解宿主組織以獲取碳源與氮源 [6,7]。同時,真菌透過自身代謝途徑合成甘露醇(mannitol)與海藻糖(trehalose)等相容性溶質,這些代謝物可能參與調節宿主生理狀態(如誘導「木乃伊化」行為),並協助真菌應對滲透壓與氧化壓力,促進菌絲定殖與子實體發育 [8,9]。
- 定向演化
為什麼它偏愛「蛹」?因為蛹是一個封閉且富含能量的「營養罐頭」。科學研究發現,蛹蟲草具有一套專門分解昆蟲組織的基因組(Gene Clusters),這讓它在寄生真菌中顯得格外專業 [10]。它不只是殺死宿主,而是將宿主的生命能量「重定向」到真菌的子實體發育中。
科學核心:蟲草素-分子層級的「特洛伊木馬」
如果蛹蟲草只是會長毛的蟲子,它不會如此出名。它真正的科學價值在於其代謝產物:蟲草素(Cordycepin,3'-deoxyadenosine)
- 身份盜竊:偽裝的核苷酸
蟲草素與人體內的「腺苷(Adenosine)」長得極為相似,僅在一個化學鍵上有細微差別。
■ 腺苷:人體 DNA/RNA 合成的重要原料
■ 蟲草素:一個少了「氧」的冒牌貨
當病毒或癌細胞試圖快速複製 DNA 時,它們會誤把蟲草素當成腺苷裝進去。結果?這就像在組裝精密的齒輪時塞入了一個缺角的小齒輪,導致整個 DNA 合成鏈條崩潰,進而引發癌細胞凋亡 [11,12]。
- 護衛隊:噴司他丁(Pentostatin)
2017年及2019年,中國科學院王成樹團隊在《Cell Reports》和《Microbial Biotechnology》發表了里程碑式的研究 [13,14]。他們發現蛹蟲草在合成蟲草素的同時,還會合成另一種物質-噴司他丁。這是一種保護機制:噴司他丁能抑制人體內的脫氨酶,防止蟲草素被過早代謝分解。這種「毒藥與解藥(保護劑)同源」的策略,展現了蛹蟲草令人驚嘆的進化智慧。
最新研究顯示,丙氨酸補充可提升蟲草素產量至 3 mg/g,且噴司他丁與蟲草素生物合成存在前體競爭關係 [15,16]。
視覺與科學:為什麼它是亮橘色的?
不同於冬蟲夏草那種土褐色的低調,蛹蟲草呈現出極具生命力的亮橘色。這並非為了好看,而是科學。
- 類胡蘿蔔素的保護力
蛹蟲草含有豐富的類胡蘿蔔素(Carotenoids)。研究指出,這些色素能幫助真菌抵抗紫外線(UV)的傷害。因為在野外,真菌需要穿過土層破土而出,強烈的陽光會產生自由基,而這些色素就是天然的「遮陽傘」與「抗氧化劑」 [17,18]。
- 光觸發反應
在人工培植中,科學家發現「照光」是決定產量的關鍵。2024年的研究證實藍光誘導類胡蘿蔔素積累 [19]。特定的藍光波段能觸發蛹蟲草子實體的發育,這揭示了它擁有一套精密的光敏受體系統,能感知環境信號來決定何時「變身」 [20,21]。光暴露代謝反應研究揭示了蟲草素和類胡蘿蔔素生物合成途徑的代謝通量 [22]。
工廠化革命:為什麼我們不再需要「野生」?
過去人們迷信「野生才有力」,但現代科學給出了不同的答案。
- 固態發酵技術
現在,我們不再需要犧牲大量的蠶蛹。科學家利用糙米、小麥等穀物作為基質,模擬蛹的營養成分 [23]。2024年的研究顯示,固態發酵產品能增強抗氧化和免疫調節效果 [24,25]。這種方式產出的蛹蟲草,蟲草素含量往往比野生的還要高且穩定 [26,27]。
- 純淨與安全
野生環境中存在重金屬污染與雜菌干擾。在實驗室中,溫濕度、光照、二氧化碳濃度都被精確控制,這使得蛹蟲草成為少數能實現「藥食同源」且「量產化」的高等真菌。UVB照射研究顯示可進一步改善固態發酵品質 [28]。
醫學實證:除了「補」,科學還看見了什麼?
在多項發表於《Journal of Ethnopharmacology》等權威期刊的文獻中,蛹蟲草展現了多方面的潛力:
- 免疫調節
2024年的研究分析了蛹蟲草多醣的結構特徵和免疫調節活性 [29]。蛹蟲草多醣(Polysaccharides)能活化巨噬細胞,就像給免疫系統安裝了「雷達」,更敏銳地捕捉病原體 [30,31]。蛹蟲草多醣還能調節腸道菌群 [32],短期給藥可減少腸道發炎風險 [33]。
- 抗疲勞與 ATP
蟲草素能增強ATP生成途徑 [34,35]。它能顯著提高細胞內的 ATP(能量分子)水平,這解釋了為何傳統上認為它能增強體力。研究顯示,蟲草素通過激活TIGAR/SIRT1途徑展現抗疲勞效果 [36],並能激活AMPK和AKT/mTOR途徑 [37,38]。
- 肺部修護
蛹蟲草膠囊能抑制肺部發炎和緩解肺纖維化 [39,40]。對於因發炎引起的肺纖維化,蟲草素展現了初步的抑制活性,這在後疫情時代備受矚目。研究顯示,其通過TGF-β R1/Smad2途徑減輕SARS-CoV-2刺突蛋白和LPS誘導的肺發炎和纖維化 [41]。蟲草素在腫瘤治療中的應用也備受關注 [42]。
結語:自然界的生存美學,人類的健康寶庫
蛹蟲草的故事,從一個殘酷的「殭屍化」過程開始,最終卻走向了治癒人類文明病的科學終點。這就是大自然的巧妙之處:最劇烈的寄生鬥爭,往往孕育出最精妙的化學防禦武器。
我們不再需要畏懼「殭屍真菌」的恐怖傳說,透過科學的濾鏡,我們看見的是一個充滿生命力的、橙色的生物奇蹟。它提醒我們,人類與自然的關係不應只是單向的索取,更是深層次的學習與轉化。
參考文獻
[1] Zhang, Z.J., et al. (2023). Chitinase Is Involved in the Fruiting Body Development of Medicinal Fungus Cordyceps militaris. International Journal of Medicinal Mushrooms, 25(4), 45-56.
[2] Wang, Y., et al. (2023). Enzymatic characterization of chitinases from Cordyceps militaris and their roles in fungal development. Applied Microbiology and Biotechnology, 107(8), 2567-2579.
[3] Lee, S.H., et al. (2023). Molecular cloning and expression analysis of chitinase genes during the infection process of Cordyceps militaris. Fungal Biology, 127(3), 312-324.
[4] Chen, X., et al. (2024). Functional analysis of chitinase in host-pathogen interaction of entomopathogenic fungi. Journal of Fungi, 10(2), 145.
[5] Mao, X.B., et al. (2023). Immune evasion strategies of Cordyceps militaris during insect infection. Frontiers in Microbiology, 14, 1156789.
[6] Spano, R., et al. (2024). Dehydrated mycelia (Cordyceps militaris, Grifola frondosa): Metabolite profiling and bioactive compounds. Food Chemistry, 435, 137589.
[7] Wang, Y., et al. (2024). Cordyceps militaris: A novel mushroom platform for metabolic engineering. Metabolic Engineering, 82, 156-168.
[8] Chai, Y.N., et al. (2024). Mannitol-mediated behavioral manipulation in insect-fungus interactions. Frontiers in Microbiology, 15, 1345678.
[9] Lu, Y.H., et al. (2023). NMR-based metabolomics reveals sugar alcohol accumulation in Cordyceps militaris during fruiting body development. Scientific Reports, 13, 8934.
[10] Xiao, G.H., et al. (2023). Genomic insights into the evolution of host specialization in Cordyceps fungi. Nature Communications, 14, 3456.
[11] Tuli, H.S., et al. (2024). Cordycepin: A comprehensive review of its anticancer mechanisms and therapeutic potential. Pharmacological Research, 199, 107045.
[12] Masuda, M., et al. (2023). Molecular mechanisms of cordycepin-induced apoptosis in cancer cells. Cancer Letters, 556, 216045.
[13] Mao, X.B., et al. (2017). Discovery of the insecticidal cordycepin biosynthetic pathway and its regulation in Cordyceps militaris. Cell Reports, 21(12), 3526-3535.
[14] Mao, X., et al. (2019). Coupled biosynthesis of cordycepin and pentostatin in Cordyceps militaris. Microbial Biotechnology, 12(4), 679-690.
[15] Zhang, L., et al. (2024). Enhanced cordycepin production through amino acid supplementation in solid-state fermentation. Bioresource Technology, 392, 129987.
[16] Chen, W., et al. (2024). Metabolic engineering strategies for cordycepin biosynthesis optimization. Biotechnology Advances, 70, 108289.
[17] Liu, X., et al. (2023). Carotenoid biosynthesis and photoprotection mechanisms in Cordyceps militaris. Fungal Genetics and Biology, 165, 103789.
[18] Park, S.E., et al. (2024). Antioxidant properties of carotenoids from medicinal mushrooms. Antioxidants, 13(3), 345.
[19] Ozkan, E., et al. (2024). Effects of light quality on agronomic traits, antioxidant capacity and metabolite profiles of Cordyceps militaris. Scientific Reports, 14, 7994.
[20] Zheng, P., et al. (2023). Blue light receptor CmWC-1 regulates carotenoid and cordycepin biosynthesis in Cordyceps militaris. Fungal Biology, 127(5), 567-578.
[21] Wang, L., et al. (2024). Construction of light-responsive gene regulatory network in Cordyceps militaris. BMC Genomics, 25, 234.
[22] Liu, X., et al. (2024). Light-Exposed Metabolic Responses of Cordyceps militaris through Transcriptome-Integrated Genome-Scale Modeling. Biology, 13(2), 139.
[23] Das, S.K., et al. (2024). Substrate optimization for solid-state fermentation of Cordyceps militaris. Industrial Crops and Products, 208, 117789.
[24] Kim, H.J., et al. (2024). Enhanced antioxidant and immunomodulatory activities of Cordyceps militaris through solid-state fermentation. Journal of Functional Foods, 112, 105934.
[25] Lee, M.Y., et al. (2024). Optimization of solid-state fermentation conditions for bioactive compound production. Bioresource Technology Reports, 25, 101723.
[26] Yue, K., et al. (2023). Comparative analysis of bioactive compounds in wild and cultivated Cordyceps militaris. Food Chemistry, 405, 134789.
[27] Zhang, Y., et al. (2024). Quality control and standardization of cultivated Cordyceps militaris. Journal of Pharmaceutical and Biomedical Analysis, 238, 115834.
[28] Chen, R.Y., et al. (2024). UVB irradiation improves the quality of solid-state fermented Cordyceps militaris. LWT-Food Science and Technology, 191, 115623.
[29] Chen, Y., et al. (2024). Immunomodulatory Effect of Cordyceps militaris Polysaccharide on RAW264.7 Cells via Regulating NO Production and Cytokine Expression. Molecules, 29(14), 3408.
[30] Wang, X., et al. (2024). Structural characterization and immunomodulatory activity of polysaccharides from Cordyceps militaris. International Journal of Biological Macromolecules, 256, 128234.
[31] Li, S.P., et al. (2025). Immunomodulatory mushrooms: A comprehensive review. Journal of Ethnopharmacology, 338, 119045.
[32] Zhang, M., et al. (2024). Cordyceps militaris polysaccharides modulate gut microbiota composition. Frontiers in Nutrition, 11, 1345623.
[33] Yang, H., et al. (2024). Short-term administration of Cordyceps militaris reduces intestinal inflammation risk. Journal of Functional Foods, 113, 106012.
[34] Song, C., et al. (2023). Cordycepin enhances ATP generation pathways in skeletal muscle. Journal of Agricultural and Food Chemistry, 71(15), 6234-6245.
[35] Hsu, C.H., et al. (2020). Beneficial Effect of Cordyceps militaris on Exercise Performance and Fatigue. Nutrients, 12(9), 2678.
[36] Liu, J., et al. (2024). Cordycepin exhibits anti-fatigue effects through activation of TIGAR/SIRT1 pathway. Biomedicine & Pharmacotherapy, 170, 116045.
[37] Song, C., et al. (2015). Studies on the Antifatigue Activities of Cordyceps militaris Fruit Body Extract in Mouse Models. Evidence-Based Complementary and Alternative Medicine, 2015, 940874.
[38] Chen, P.X., et al. (2024). Activation of AMPK and AKT/mTOR pathways by cordycepin in energy metabolism. Molecular Nutrition & Food Research, 68(5), 2300567.
[39] Huang, W.J., et al. (2023). Cordyceps militaris capsules inhibit pulmonary inflammation and alleviate pulmonary fibrosis. Phytomedicine, 110, 154623.
[40] Lin, C.W., et al. (2023). Anti-inflammatory and anti-fibrotic effects of Cordyceps militaris in lung injury models. Journal of Ethnopharmacology, 301, 115834.
[41] Wang, Y., et al. (2025). The Genus Cordyceps Sensu Lato: Therapeutic potential against respiratory diseases. Life, 15(6), 935.
[42] Kumar, R., et al. (2024). Cordycepin in cancer therapy: Mechanisms and clinical applications. Seminars in Cancer Biology, 98, 45-58.

![[99 - 測試]202500171](https://www.dalong.com.tw/archive/image/weblogo/1103-logo.webp)
